
به منظور کاهش و یا حذف کامل املاح آب از جمله یون های سختی کلسیم و منیزیم، کاتیون های فلزات سنگین مانند آهن و منگنز، نیترات، سولفات، کلر و فلوراید، کل جامدات محلول (TDS) و تولید آب بدون یون و خالص یا Demin Water، از فرآیند تبادل یونی استفاده می شود.
تبادل یونی برای موارد صنعتی از سال 1910 و با معرفی واحدهای سختی گیر آب با استفاده از زئولیت های طبیعی و زئولیت های سنتزی استفاده می شود. برخی از کانی های طبیعی مانند زئولیت ها دارای قابلیت تبادل یونی هستند. زئولیت ها نوعی رزین معدنی به شمار می آیند که می توانند سختی آب (شامل یون های کلسیم و منیزیم) را حذف کرده و یون سدیم در محیط آزاد کند. به دلیل تبادل یونی سدیم با یون های سختی آور آب، این مواد به عنوان زئولیت های سدیمی نیز شناخته می شوند. زئولیت های طبیعی به عنوان نوعی رزین تبادل یونی معدنی و طبیعی از دیرباز برای تصفیه و حذف یون های آب استفاده شده است.


رزین های تبادل یونی
رزین های تبادل یونی جایگزین مناسب تر و قابل انعطاف تری نسبت به زئولیت های طبیعی یا مصنوعی هستند. رزین تبادل یونی آنیونی و کاتیونی برای حذف یون های نامطلوب از محلول ها و گازها در فرایندهای مختلف مانند تصفیه آب (در تجهیزات سختی گیر و دیونایزر)، تصفیه فاضلاب، حذف نیترات از منابع آبی آلوده، جداسازی کروماتوگرافیک، خشک کردن مواد، فرایندهای خالص سازی در صنایع دارویی و … به کار می رود. فرایند تبادل یونی به تعویض یون ها بین ماده جامد رزین و محیط مایع گفته می شود که در آن تغییر پایدار در ساختار رزین جامد روی نمی دهد و فرایند برگشت پذیر می باشد. رزین های مبادله کننده یون برای تصفیه آب و فاضلاب و جداسازی مواد نامطلوب در بسیاری از فرایندها استفاده می شود.
رزین های تبادل یونی به دلیل مزایای زیر برای حذف آلودگی ها مناسب می باشند:
1- رزین های تبادل یونی ظرفیت و بازدهی بالایی برای حذف یون های با غلظت های پایین دارند.
2- رزین ها پایدار هستند و می توانند به راحتی بازیافت شوند.
3- رزین ها در محدوده گسترده ای از دما پایدار هستند.
4- رزین های تبادل یونی در واحدهای کوچک و بزرگ قابل استفاده است.
5- فرایند تبدل یونی با استفاده از رزین های کاتیونی و انیونی، فرایندی برگشت پذیر است.

رزین های تبادل یونی عمدتا مواد پلیمری غیرمحلولی هستند که با روش پلیمریزاسیون تعلیقی (Suspension Polymerization) با استفاده از استایرن (Styrene) و دی وینیل بنزن (Divinylbenzene, DVB) ساخته می شود و حامل گروه های عاملی قابل تبادل می باشند. این یون ها می توانند با مقدار معادل استوکیومتری از یون هایی با بار مشابه در محیط مبادله و جایگزین شوند.
در فرایند تولید رزین های تبادل یونی آنیونی و کاتیونی ترکیبات آلی پلیمریزه می شوند تا ماتریکس سه بعدی متخلخلی تشکیل دهند. یک ماده شیمیایی به عنوان عامل ایجاد پیوندهای متقابل در طی فرایند پلیمریزاسیون (Polymerization) اضافه می شود (مانند دی وینیل بنزن) تا ساختار سه بعدی رزین تولید شود. در نهایت رزین به صورت شیمیایی فعال می شود که شامل واکنش ماتریکس پلیمری با ترکیبی است که حاوی گروه عاملی با قابلیت تعویض یونی می باشد (مانند سولفوریک اسید که گروه عاملی سولفونیک را به همراه دارد).
رزین های تبادل یونی شامل رزین های کاتیونی، رزین های آنیونی و رزین های کیلاتی (Chelating Resin) می باشد. رزین های کیلاتی عملکردی مشابه رزین های کاتیونی ضعیف دارند اما انتخاب گری بالایی نسبت به کاتیون فلزات سنگین دارد. توضیحات بیشتر در خصوص انواع رزین ها در ادامه آورده شده است.

انواع رزین های تبادل یونی آنیونی و کاتیونی
رزینها برحسب گروه عامل تعویض متصل به پایه پلیمری رزین به چهار دسته تقسیم میشوند:
رزین های کاتیونی قوی، Strong Acidic cation (SAC)
رزین های کاتیونی ضعیف، Weak Acidic Cation (WAC)
رزین های آنیونی قوی، Strong Basic Anion (SBA)
رزین های آنیونی ضعیف، Weak Basic Anion (WBA)
رزین های تبادلی شامل دو دسته کلی رزین های تبادلی کاتیونی و رزین های تبادل آنیونی می باشند. رزین های حاوی کاتیون های قابل تبادل، رزین کاتیونی نامیده می شوند و رزین های حاوی آنیون های قابل تبادل، به عنوان رزین های آنیونی شناخته می شوند. رزین های آنیونی جذب یون های منفی و رزین های کاتیونی جذب یون های مثبت را بر عهده دارند.

رزین های کاتیونی هیدروژنی تمام کاتیون های آب همچون کلسیم، منیزیم، پتاسیم، آهن و… و رزین های آنیونی تمام آنیون های آب شامل سیلیس، سولفات، کلراید، نیترات و … را حذف مینمایند، در نتیجه با استفاده از هر دو نوع رزین می توان آب بدون یون تولید کرد.
به صورت کلی رزین های تبادل یونی قوی در محدوده وسیعی از pH عمل می کنند اما رزین های تبادل یونی ضعیف در محدوده کوچکی از pH مناسب هستند. رزین های یونی قوی دارای گروه های عاملی بسیار یونیزه شده هستند و در نتیجه می توانند در هر pH به راحتی گروه H+ یا OH- خود را مبادله کنند. رزین های تبادل یونی ضعیف مانند اسید ها و بازهای ضعیف مقداری یونیزه شده اند، مگر اینکه در pH بالای 7 (برای رزین کاتیونی اسیدی ضعیف) و یا زیر 7 (برای رزین آنیونی بازی ضعیف) قرار گیرند.
گروه های عاملی که در رزین های تبادل یونی وجود دارند به شرح زیر هستند:
– رزین تبادل یونی کاتیونی اسیدی قوی: گروه عاملی سولفونیک (R-SO^3H)
– رزین تبادل یونی آنیونی بازی قوی: گروه عاملی آمونیوم (R-R^3N+OH-)
– رزین تبادل یونی کاتیونی اسیدی ضعیف: گروه عاملی کربوکسیل (R-COOH)
– رزین تبادل یونی آنیونی بازی ضعیف: گروه عاملی آمین (R-NH^3OH)

رزین تبادل یونی کاتیونی (Acid Cation Exchange Resin) چیست؟
رزین های حاوی کاتیون های قابل تبادل، رزین کاتیونی نامیده و به دو دسته عمده رزین کاتیونی قوی و رزین کاتیونی ضعیف تقسیم می شوند. در هنگام انجام عملیات حذف آلاینده های آب، با استفاده از رزین کاتیونی یون هیدروژن و سدیم جایگزین کاتیون های موجود در آب می شود. در هنگام احیا رزین کاتیونی، کاتیون های سطح رزین وارد محلول احیا شده و مجددا هیدروژن و سدیم جایگزین آن ها می شود.
از رزین های پرمصرف کاتیونی موجود در ایران می توان به رزین تبادل یونی کاتیونی پرولایت C100 (PUROLITE Cation Exchange C100)، رزین تبادل یونی کاتیونی پرولایت C100E (PUROLITE Cation Exchange C100E) و رزین تبادل یونی کاتیونی C100H (PUROLITE Cation Exchange C100H) برای کاربرد در دستگاه های دیونایزر اشاره کرد.
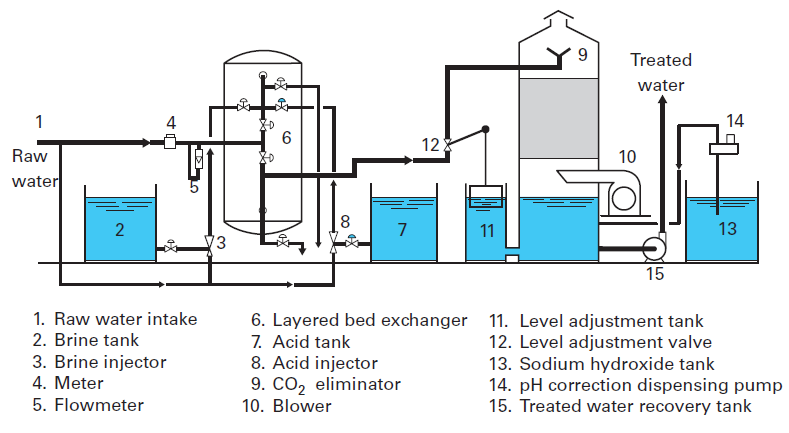
رزین کاتیونی اسیدی قوی (Strong Acidic Cation Resin)
رزین کاتیونی قوی قابلیت جذب تمامی کاتیون های موجود در محلول و آب را دارد. پرمصرف ترین رزین کاتیونی در صنعت آب و فاضلاب رزین کاتیونی سدیمی می باشد که جهت سختی گیری آب و حذف یون های کلسیم و منیزیم استفاده می شود.
رزین های اسیدی قوی رفتاری مشابه اسیدهای قوی دارند. رزین هایی بر پایه پلی استایرن به همراه گروه سولفونیک اسید (-SO^3H) به عنوان گروه عاملی هستند و از نظر ساختاری در دو فرم هیدروژنی با فرمول شیمیایی R-SO^3H و فرم سدیمی با فرمول شیمیایی R-SO^3Na موجود می باشند. واکنش تبادل در رزین کاتیونی اسیدی قوی به صورت زیر است:
![]()
رزین های کاتیونی اسیدی قوی برای حذف سختی آب و حذف مواد معدنی آب استفاده می شود. رزین کاتیونی قوی می تواند با تمامی کاتیون ها تبادل یونی داشته باشد و ظرفیت تبادل یونی آن وابسته به pH نمی باشد. رزین های کاتیونی قوی مصرف شده قابل بازیابی و احیا هستند. احیا در فرم هیدروژنی با استفاده از یک اسید قوی (مانند HCl) و احیا در فرم سدیمی با استفاده از محلول سدیم کلرید (NaCl) انجام می شود.

رزین کاتیونی اسیدی ضعیف (Weak Acidic Cation Resin)
رزین های کاتیونی ضعیف قادر به جذب کاتیون های مرتبط با قلیاییت آب می باشند و همه کاتیون های موجود در محلول را نمی توانند جذب نمایند. رزین کاتیونی ضعیف بر پایه اکرلیک به همراه گروه کربوکسیلیک اسید (-COOH) به عنوان گروه عاملی هستند و فرم هیدروژنی و ساختار R-COOH دارند. رزین های کاتیونی اسیدی ضعیف رفتاری مشابه اسیدهای ضعیف دارند و مشابه اسیدهای ضعیف به مقدار جزئی تجزیه می شوند. این رزین ها می توانند در کنار رزین های کاتیونی قوی استفاده شده و بازدهی بالایی در حذف حاصل کنند. واکنش تبادل در رزین کاتیونی اسیدی ضعیف به صورت زیر است:
![]()
مزیت رزین های کاتیونی ضعیف بازدهی بالای آنها در مقایسه با رزین های کاتیونی قوی است، در نتیجه باعث تولید پساب کمتر در احیاهای مکرر می شود. رزین های کاتیونی ضعیف می توانند سختی مرتبط با قلیاییت را حذف کند. بازیافت و بازیابی رزین های کاتیونی ضعیف با بازدهی بالا قابل انجام است. رزین های کاتیونی ضعیف تمایل بالایی نسبت به یون های هیدروژن دارند و در نتیجه احیای آنها به سادگی با استفاده از مقدار استوکیومتری از اسید صورت می گیرد.
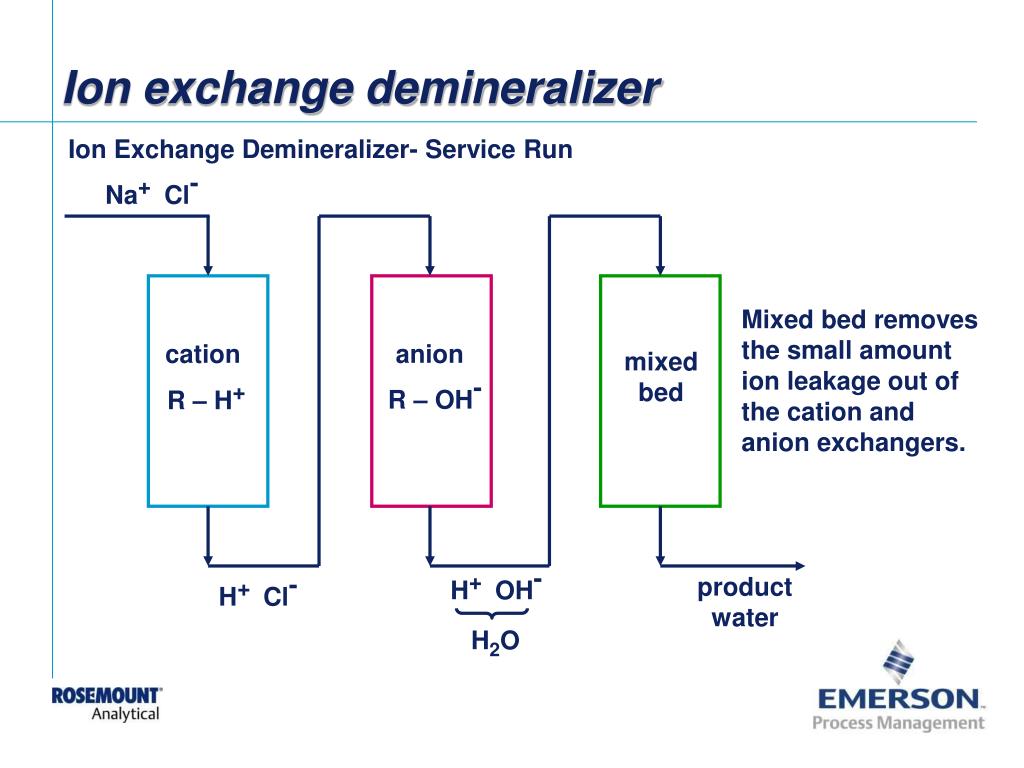
رزین تبادل یونی آنیونی (Base Anion Exchange Resin) چیست؟
رزین های حاوی آنیون های قابل تبادل، به عنوان رزین های آنیونی شناخته و به دو دسته عمده رزین انیونی قوی و رزین انیونی ضعیف تقسیم می شوند.
از رزین های پرمصرف آنیونی موجود در ایران می توان به رزین تبادل یونی آنیونی پرولایت A400 (PUROLITE Anion Exchange A400) برای کاربرد در دستگاه های دیونایزر اشاره کرد.
رزین آنیونی بازی قوی (Strong Base Anion Resin)
رزین های تبادل آنیونی قوی قابلیت حذف تمامی آنیون ها از آب را دارد. رزین های تبادل آنیونی قوی بر اساس ماهیت گروه های عاملی و نوع آمین مورد استفاده در طی فرایند فعال سازی شیمیایی به دو دسته کلی نوع (I) و نوع (II) تقسیم می شوند. در نوع (I) در گروه عاملی آمونیوم سه گروه متیل وجود دارد درحالیکه در نوع (II) یکی از گروه های متیل با گروه اتانول جایگزین شده است. واکنش تبادل در رزین آنیونی بازی قوی به صورت زیر است:
![]()

رزین آنیونی بازی ضعیف (Weak Base Anion Resin)
رزین های آنیونی ضعیف قابلیت جذب آنیون اسیدهای قوی مانند اسید سولفوریک، کلریدریک اسید و نیتریک اسید را دارد. این رزین ها آنیون هایی مرتبط با اسیدهای معدنی را می توانند حذف کنند اما قادر به حذف آنیون های مرتبط با اسیدهای ضعیف (مانند کربنیک اسید، سیلیسیک اسید) نمی باشند. همچنین این رزین ها نمی توانند سیلیکا را از آب حذف کند. این رزین ها مقاوم تر از رزین آنیونی قوی بوده و به همین جهت در سیستم های تصفیه آب کاربرد بیشتری دارند.
رزین تبادل آنیونی ضعیف دارای گروه عاملی آمین است. خاصیت بازی و قلیاییت بسیار کمتری نسبت به رزین آنیونی قوی دارد. واکنش تبادل در رزین آنیونی بازی ضعیف به صورت زیر است:
![]()
رزین های آنیونی ضعیف با استفاده از مقدار استوکیومتری از عامل احیاکننده مجددا بازیابی شود.

رزین بستر مختلط (Mixed Bed Ion Exchange Resin)
رزین بستر مختلط در مواردی که کیفیت بسیار بالای آب خروجی مدنظر می باشد مورد استفاده قرار می گیرد. در واحد بستر مختلط پولیشر (Mixed Bed Polisher) مخلوطی از رزین اسیدی کاتیونی قوی به فرم هیدروژنی و رزین بازی آنیونی قوی به فرم هیدروکسید استفاده می شود. معمولا خروجی رزین آنیونی قوی از رزین بستر مختلط عبور داده می شود تا کیفیت آب بهبود یابد.

رزین حذف نیترات (Nitrate Selective Ion Exchange Resin)
نیتروژن یکی از عناصر اصلی تشکیل دهنده ارگانیسم های زنده می باشد. با این وجود آزادسازی بیش از حد نیتروژن در محیط زیست منجر به مشکلات جدی محیط زیستی مانند اوتریفیکاسیون شود. همچنین مصرف آبهای آلوده به نیترات آثار زیان باری مانند بیماری متهموگلوبینمیا (Methemoglobinemia)، سندرم کودک آبی (Blue baby syndrome)، اختلال در تیروئید، گواتر، سرطان و سقط جنین های خود به خود را در پی دارد.
رزین های آنیونی قوی نوع یک و نوع دو جذب سولفات را به جذب نیترات ترجیح می دهند. تمایل بیشتر به جذب سولفات نسبت به نیترات منجر به تجمع نیترات (Nitrate dumping) در آب و فاضلاب می شود. برای برطرف کردن این مشکل، رزین های حذف انتخابی نیترات تولید می شوند که انتخاب پذیری نیترات در آنها بیشتر از سولفات و سایر آنیون ها حتی در TDS بسیار پایین می باشد و مانع از تجمع نیترات در محلول می شود.
رزین کاتیونی سختی گیر (Calcium and Magnesium Selective Ion Exchange Resin)
رزین های کاتیونی سختی گیری به صورت انتخابی به حذف یون های سختی شامل کلسیم و منیزیم می پردازد. رزین پرولایت برای حذف انتخابی کلسیم و منیزیم از شیرآبه، از نوع رزین های کیلاتی با گروه عاملی آمینوفسفونیک است. ساختار شیمیایی رزین انتخابی سختی گیری، تمایل بیشتری نسبت به کاتیون های کلسیم و منیزیم داشته و کمپلک های پایدارتری با انها تشکیل می دهد و در نتیجه تشکیل کمپلکس با یون های کلسیم و منیزیم نسبت به سایر یون ها را تسهیل می کند.
رزین حذف آهن و منگنز (Iron and Manganese Selective Ion Exchange Resin)
این نوع رزین برای حذف انتخابی فلزات سنگین شامل آهن و منگنز تولید می شود. رزین انتخابی حذف آهن ومنگنز از نوع رزین های کیلاتی (chelating) از جنس پلی استایرن و با ساختار متخلخل و حفرات ماکرو است و دارای گروه عاملی ایمینو دی استیک است که برای حذف کاتیون های فلزات سنگین از فاضلاب های صنعتی طراحی شده است. رزین انتخابی حذف فلزات سنگین اهن و منگنز در فرایندهایی شامل استخراج و بازیافت فلزات از سنگ معدن، تصفیه فاضلاب آبکاری ها، و حمام آبکاری فلزات کاربرد دارد.
رزین حذف آرسنیک (Arsenic Selective Ion Exchange Resin)
به دلیل قدرت یونی پایین یون آرسنیک، ظرفیت رزین های عمومی برای جذب آرسنیک در میان یون های دیگر پایین می باشد. یون آرسنیک بسیار سمی می باشد و در صورت حذف نشدن خطرات بالایی مانند بیماری سرطان ایجاد می نماید. از این رو رزین هایی با خاصیت جذب انتخابی آرسنیک تولید می شوند.

رزین حذف بور (Boron Selective Ion Exchange Resin)
رزین انتخابی بور (Boron Selective Resin) نوعی از رزین تبادل یونی آنیونی ضعیف است که می تواند بور را حتی در غلظت های بسیار پایین و در حضور سایر یون ها جذب کند. رزین حذف بور دارای گروه عاملی n-methyl-D-glucamine است که انتخاب پذیری بسیار بالایی نسبت به بور دارد. رزین انتخابی بور دارای کمپلکس حلقوی از بورات استر است که در زیر نشان داده شده است و بور را به خود جذب می نماید.
شرکت های تولیدکننده رزین های تجارتی، رزین های تبادل یونی را برای مصارف مختلف و با ویژگی های گوناگون تولید می کنند. از میان آنها می توان به رزین کاتیونی و آنیونی پرولایت (PUROLITE ion exchange resin)، رزین تبادل یونی آمبرلایت (AMBERLITE ion exchange resin)، رزین تبادل یونی آمبرجت (PUROLITE AMBERJET ion resin)، رزین بایر آلمان (Bayer ion exchange resin)، رزین لواتیت (LEWATIT ion exchange resin)، رزین داو (DOW ion exchange resin)، رزین روم اند هاس (Rohm and Haas ion exchange resin) و … اشاره کرد.
کاربردهای رزین تبادل یونی
انتخاب رزین مناسب بر اساس کیفیت مورد نظر برای آب انجام می شوند و سپس در ستون های مورد نظر قرار می گیرند. کاربردهای گسترده رزین های تبادل یونی شامل موارد زیر می شود:
– حذف سختی آب و در تجهیزات سختی گیری آب
– دی یونیزه کردن کامل آب توسط رزین میکس بد (Mixed Bed)
– دی آلکالیزاسیون (Dealkalization) و یا حذف جزئی مواد معدنی (Partial Demineralization)
– حذف مواد معدنی (همراه و یا بدون حذف سیلیکا)
– بستر مختلط (Mixed Bed)
– حذف نیترات و فلوراید
– حذف فلزات سنگین
– حذف رنگ، مواد آلی
– جداسازی کروماتوگرافیک
– کاربردهای فرایندی
– نایع دارویی و خالص سازی مواد
– صنایع غذایی و نوشیدنی
– حذف و بازیافت رنگ در صنعت نساجی
– نیروگاه ها
– نیروگاه های هسته ای
– بازیابی و جداسازی فلزات باارزش
– کاربرد به عنوان کاتالیست در برخی فرایندها
– فرایند تصفیه بیو دیزل
ویژگی های فیزیکی رزین های تبادل یونی
مواد تبادل یونی به فرم کروی و یا گاهی گرانول با اندازه و یکنواختی مشخصی برای کاربردهای گوناگون تولید می شوند. بیشتر رزین های تبادل یونی به فرم کروی هستند و توزیع اندازه ذراتی بین 0/3 الی 1/2 میلیمتر (مش 50-16) دارند. رزین ها در حالتی که با آب متورم شده باشند، وزن مخصوصی برابر با 1/1- 1/5 دارند. چگالی بالک برای محصولات رزینی خیس عموما در محدوده g/L 560- 960 (lb/ft^3 35- 60) می باشد.
ویژگی های شیمیایی رزین های تبادل یونی
1- تورم پذیری رزین تبادل یونی: رزین های تبادل یونی تمایل به جذب رطوبت دارند. مقدار رطوبت جذب شده توسط رزین تبادل یونی به پیوندهای متقابل و گروه عاملی در ساختار آن وابسته می باشد. رزین های ژله ای با پیوندهای متقابل کم و گروه های عاملی سولفونیک اسید یا آمونیوم، محتوی مقادیر زیادی آب هستند که منجر به تورم آنها می شود. تورم و انقباض های پی در پی موجب کاهش عمر رزین تبادل یونی می شود.
2- ظرفیت رزین تبادل یونی: طرفیت تبادل یونی برابر است با تعداد یون هایی که توسط یک واحد وزنی (وزن خشک/ وزن تر) و یا حجمی (حجم تر) از رزین جذب می شوند. در اندازه گیری طرفیت رزین بر پایه وزن خشک، وجود پیوندهای متقابل در ساختار رزین تبادل یونی موجب کاهش گروه های عاملی چسبیده به سطح و در نتیجه کاهش ظرفیت می شود.
3- اندازه ذره در رزین تبادل یونی: رزین های تبادل یونی در اندازه ذرات و اندازه بستر مختلف ارائه می شوند. رزین های تبادل یونی متداول به فرم بسترهای کروی پلی دیسپرس با توزیع اندازه ذرات بین 0/25 – 1/25 میلیمتر و یا اندازه ذرات یکنواخت تولید می شوند. ذرات کوچکتر سینتیک واکنش تبادل یونی را بهبود می دهند اما منجر به افزایش افت فشار آب و کاهش شدت جریان می شوند.
4- پایداری رزین تبادل یونی: پایداری مکانیکی یا پایداری فیزیکی رزین های تبادل یونی عمدتا تحت تاثیر سختی ساختار پلیمری و تناوب سیکل های تورم و انقباض در رزین های تبادل یونی می باشد. عواملی مانند ته نشین شدن مواد (مانند هیدروکسید آهن) و گرفتگی حفرات رزین تبادل یونی، شکستن ساختار پلیمری رزین تبادلی، تغییر شکل گروه های عاملی و در نتیجه کاهش ظرفیت تبادل یونی منجر به تجزیه شیمیایی رزین های تبادل یونی می شود.
معیارهای ارزیابی عملکرد رزین های تبادل یونی
رزین های تبادل یونی کاربردهای گسترده و مختلفی دارند. بنابراین معیارها و ضوابطی که بر عملکرد رزین های تبادل یونی حاکم هستند باید در انتخاب توع رزین مناسب برای فرایند در نظر گرفته شوند. معیارهای رزین تبادل یونی مناسب در ادامه آورده شده است:
– رزین تبادل یونی در آب و محلول های آلی غیر محلول باشد و همچنین در محیط های اسیدی، بازی و اکسیدکننده مختلف پایدار باشد.
– رزین تبادل یونی باید از نظر فیزیکی سخت باشد تا قادر به تحمل تنش و فشار مکانیکی باشد.
– ساختار مولکولی رزین تبادل یونی در مقابل یون ها و مولکول های حلال باز باشد به صورتیکه مولکول ها و یون ها بتوانند در طی فرایند تبادل یونی وارد و خارج شوند.
– پایداری حرارتی رزین تبادل یونی بالا باشد تا در فرایندهایی که در دمای بالا انجام می شود بازدهی و عملکرد مناسب ارائه نماید.
– بازیابی و احیای رزین تبادل یونی بدون افت محسوس عملکرد آن قابل انجام باشد.
تبادل یونی
فرایند تعویضو تبادل یونی از زمان قدیم مورد استفاده قرار می گرفت. ارستا تالیس به کمک این فرایند آب شور را با خاک هایی تماس می داد و آب شیرین تهیه می کرد.
در سال 1845 تامسون نشان داد که هر گاه آب حاوی آمونیوم سولفات از خاک عبور کند در آب خروجی کلسیم سولفات تولید خواهد شد.
NH4)2Z + CaSO4) → (خاک کلسیم دار)NH4)2SO4 + CaZ)
این شناسایی سر آغاز پیشرفت دانش تبادل یونی گردید و در نیمه دوم قرن نوزدهم نشان داده شد که ترکیباتی از فلزات قلیایی خاکی، سیلیس و آلومینیوم به نام آلومینوسیلیکات ها (Al2O3 / mNa2O / xSiO2 / yH2O) قادر به مبادله یونی می باشند. مواد معدنی که دارای بیشترین ظرفیت تعویض یونی بودند، خاک های دیاتومه و نوعی شن های سبز رنگ بودند که زئولیت خوانده می شدند.
در سال 1930 اولین مبادله کننده های یونی از واکنش آنتراسیت و سولفوریک اسید ساخته شدند که به نام ذغال سولفونه شده معروف گردیدند. بیشترین ظرفیت این تبادل کننده های یونی حدود 0.7eq kg-1 می باشد. سپس رزین های تبادل کننده ی یونی پلیمری از ترکیب فنل و یا مشتقات آن با فرمالدئید ساخته شد که ظرفیت آنها حدود 1.2eq kg-1 بود. در ادامه این بررسی ها رزین های مختلفی ساخته شد و بالاخره در سال 1945 به کمک کوپلیمریزاسیون استایرن و دی وینیل بنزن، رزین های کروی شکل کاتیونی و آنیونی ضعیف و قوی تهیه گردیدند که ظرفیت این رزین ها گاهی تا چند برابر انواع قبلی می رسد.

پدیده تبادل یونی
رزین های تعویض یونی، جامدات نامحلول در آب می باشند که به وسیله تبادل یون می توانند جهت جذب کاتیون ها و آنیون ها به کار گرفته شوند. پدیده تعویض یون ترکیبی از پدیده جذب سطحی و فرایند نفوذ می باشد و سرعت واکنش را عملیات انتقال جرم که یون ها را از سیال به سطح رزین و یا از سطح رزین به سیال می رساند مشخص می کند.
پدیده تبادل یون یک تعادل شیمیایی است و از اصول حاکم بر تعادل ها پیروی می کند. در الکترولیت ها نیز پدیده تعویض یون وجود دارد ولی به دلیل همگن بودن یون ها که در آن مبادله کننده های یون هر دو مایع می باشند عامل موثر سینتیک شیمیایی است در حالی که در تعویض یونی به دلیل وجود نیروهای الکتروستاتیک می باشد و قدرت تبادل به این نیروها بستگی دارد که میزان آن ها بر اساس محاسبات استوکیومتری نمایش داده می شود و به شیوه ای است که مواد قبل و بعد از تبادل یون هر دو از نظر الکتریکی خنثی خواهند بود.

برخی رزین های کاتیونی دارای گروه فعال کربوکسیل (─COOH) می باشند که فقط با کاتیون های اسیدهای ضعیف تبادل یونی می نمایند. برای مثال چنانچه تمام قلیائیت یک آب بی کربناتی مربوط به املاح کلسیم و منیزیم باشد در این صورت تبادل یون به شکل زیر نمایش داده می شود.
Ca(HCO3) + H2R → CaR + 2CO2 +2H2O
Mg(HCO3)2 + H2R → MgR + 2CO2 + 2H2O
تبادل یون انجام نمی شود → CaSO4 + H2R
تبادل یون انجام نمی شود → MgCl2 + H2R
آب تولید شده دارای سختی بسیار کمتری است. مزایای این نوع رزین ها عبارتند از:
الف) ظرفیت بالا
ب) احیا با اسید کمتر و رقیق تر
پ) نیاز به آب کمتر برای آب کشی
جهت تولید آب بدون یون از رزین های کاتیونی و آنیونی استفاده می گردد. این رزین ها در انواع ضعیف و قوی تولید می شوند. رزین های کاتیونی قوی توانایی حذف کلیه کاتیون ها را دارا می باشند.
H2R + CaCl2 ↔ CaR + 2HCl
H2R + 2NH2NO3 ↔ (NH4)2R + 2HNO3
H2R + K2R + H2SO4 ↔ K2R + H2SO4
H2R + Na2SO4 ↔ Na2R + H2SO4
آنیون های قوی موجود در آب نیز با رزین های تبادل یونی آنیونی تبادل یون می کنند. فرآیند تبادل آنیون به صورت زیر نمایش داده می شود.
R(OH)2 + H2SO4 ↔ SO4R + 2H2O
R(OH)2 + 2HCl ↔ Cl2R + 2H2O
R(OH)2 + 2HNO3 ↔ (NO3)2R + 2H2O
رزین های کاتیونی (Cationic resins)
رزین های کاتیونی در اثر واکنش فنل و یا مشتقات آن با فرمالدئید و سپس سولفونه کردن آنها به کمک سولفوریک اسید به حالت توده ای تهیه شدند که آنها را خرد و غربال می کردند و مورد استفاده قرار می دادند. این گونه رزین ها نیز از سولفونه کردن پلی استیرن تهیه گردیدند.

هرگاه در پلیمریزاسیون استایرن مقداری دی وینیل بنزن افزوده گردد پلیمری با ساختار شبکه ای تولید می گردد که در اثر سولفونه کردن آن، رزین کاتیونی قوی تهیه می گردد.
با تغییر دادن میزان دی وینیل بنزن درجه cross-linked و در نتیجه تخلخل و پایداری رزین کنترل می گردد. افزایش پیوندهای متقاطع موجب کاهش تخلخل می شود و در نتیجه مقاومت دمایی رزین بالا می رود.
برای تولید دانه های کروی باید به کمک همزن، منومر در درون آب به حالت سوسپانسیون در آید و در این شرایط کوپلیمریزاسیون انجام گیرد. رزین های کاتیونی قوی می توانند با تمام کاتیون های موجود در آب تبادل یون نمایند.

هرگاه به جای گروه سولفونیک اسید گروه کربوکسیلیک اسید (─COOH) جانشین شود رزین های کاتیونی ضعیف تولید میگردد ولی روش ساده تر برای تهیه این رزین ها ترکیب متاکریلیک اسید با دی وینیل بنزن می باشد. به طور معمول ظرفیت رزین های کاتیونی ضعیف بیشتر از ظرفیت انواع قوی می باشد که این میزان گاهی به دو برابر می رسد.

رزین های آنیونی (Anionic resins)
رزین های آنیونی به جای گروه های اسید دارای گروه های بازی می باشند. گروه های بازی از آمونیاک و یا یک آمین ایجاد می شوند و برای داشتن شرایط بهتر می توان از ترکیبات دیگری مانند گروه های کلرومتیل استفاده نمود و سپس واکنش با آمونیاک و یا آمین تکمیل گردد.
الف) در اثر واکنش با آمونیاک رزین آنیونی، آمین نوع اول تهیه می گردد.
ب) در اثر ترکیب با یک آمین نوع اول رزین آنیونی آمین نوع دوم تهیه می گردد.
پ) در اثر واکنش با یک آمین نوع دوم رزین آنیونی آمین نوع سوم تهیه می گردد.
ت) در اثر واکنش با یک آمین نوع سوم رزین آنیونی آمونیومی تولید می گردد.
رزین های دارای گروه های بازی آمین نوع اول، دوم و سوم از نوع ضعیف می باشند و توانایی تبادل یون با آنیون های نمک ها یا اسیدهای قوی را دارا می باشند ولی با آنیون های نمک ها و یا اسیدهای ضعیف تبادل یون نمی نمایند.
تبادل یون انجام می شود↔ SO42- + رزین های آنیونی ضعیف
تبادل یون انجام می شود↔ NO3– + رزین های آنیونی ضعیف
تبادل یون انجام می شود↔ Cl– + رزین های آنیونی ضعیف
تبادل یون انجام نمی شود↔ HSiO3– + رزین های آنیونی ضعیف
تبادل یون انجام نمی شود↔ HCO3– + رزین های آنیونی ضعیف
رزین های آمونیومی از نوع قوی می باشند و توانایی تبادل یون با همه آنیون ها حتی بنیان کربنیک اسید و بنیان سیلیسیک اسید را دارند.
تبادل یون انجام می شود↔ HSiO3– + رزین های آنیونی قوی
تبادل یون انجام می شود↔ HCO3– + رزین های آنیونی قوی
به طور معمول رزین های آنیونی ضعیف با سدیم کربنات یا سود سوزآور احیا می شوند ولی احیای آنها با بیشتر قلیاها امکان پذیر خواهد بود.
RCl2 + Na2CO3 +H2O → R(OH)2 + 2NaCl + CO2
احیای رزین های آنیونی قوی با سدیم هیدروکسید انجام می پذیرد.
RCl2 + 2NaOH → R(OH)2 + 2NaCl
رزین های تبادل یونی ویژه بستر مختلط (Mixed bed columns ion-exchange resins)
حذف کاتیون ها و آنیون های موجود در آب، به طور همزمان به وسیله مخلوطی از رزین های تبادل یونی کاتیونی و آنیونی انجام می گیرد. در این فرآیند مخلوط رزین ها در یک ستون قرار می گیرند و آب از بستر رزین ها عبور می کند و آب خروجی دارای T.D.S. بسیار ناچیزی خواهد بود.
احیای رزین های کاتیونی و آنیونی در چند مرحله انجام می پذیرد. در نخستین مرحله رزین ها به شیوه مکانیکی از یکدیگر جدا می شوند،سپس رزین ها احیا می گردند و در مرحله نهایی دو رزین کاتیونی و آنیونی مخلوط می شوند و مورد استفاده قرار می گیرند.
مزیت های روش تبادل یونی
روش تبادل یونی در مقایسه با سایر روش ها از مزایای زیر برخوردار است.
الف) سهولت در نصب و بهره برداری.
ب) بالا بودن عمر مفید رزین ها (در شرایط بهره برداری مناسب عمر رزین ها بیشتر از 15 سال است).
پ) قابلیت اجرا در ظرفیت های مختلف.
ت) عدم وجود فاضلاب آلوده برای محیط زیست.
محدودیت های روش تبادل یونی
در کنار مزایای روش تبادل یونی محدودیت هایی نیز به شرح زیر وجود دارند:
الف) در محدوده ی T.D.S. > 700 ppm مقرون به صرفه نیست.
ب) این روش برای واحدهای صنعتی متداول می باشد و معمولا برای آب آشامیدنی مورد استفاده قرار نمی گیرد.
پ) مواد شیمیایی مصرفی از همه روش ها بیشتر و آب تولیدی پر هزینه تر است.
ت) دمای فرایند تبادل یونی نباید از 10 ◦C کمتر باشد.
ث) بر اساس نوع رزین و پوشش ستون تبادل یونی ماکزیمم دمای فرایند تبادل یونی محدودیت دارد.
ج) اجسام غیر یونیزه قابلیت تبادل یونی ندارند.
چ) حد مجاز آهن، منگنز و فلزات سنگین در مجموع باید کمتر از 0.1 ppm باشد.
ح) آب عبوری از رزین های تبادل یونی باید فاقد املاح معلق، اجسام کلوئیدی، چربی و مواد آلی باشد.
خ) حد مجاز کلرین (ClO–) آزاد آب عبوری 0.05ppm می باشد.
د) حد مجاز کدورت 5A.P.H.A. Units می باشد.
Cause-effect diagram for short runs in a two-bed demineralizer system.


